Korozyon Nedir? Korozyon Çeşitleri, Etkileri, Önlenmesi
Korozyon Nedir? Korozyon Çeşitleri, Etkileri, Önlenmesi
- BİLİM ve TEKNOLOJİ
- Tue, 9 Jul 2024 16:05:24
- Tue, 9 Jul 2024 16:05:24
Korozyon, günlük hayatımızda en sık gözlemlediğimiz olaylardan biridir. Demirden yapılmış bazı nesnelerin bir noktada turuncu veya kırmızımsı kahverengi renkli bir tabaka ile kaplandığını fark etmiş olmalısınız. Bu tabakanın oluşumu, bir korozyon şekli olan paslanma olarak bilinen kimyasal bir sürecin sonucudur.
Cossorion, genel olarak, rafine metallerin metal oksitler, metal sülfürler veya metal hidroksitler gibi daha kararlı bileşiklere dönüştürüldüğü bir işlemdir. Benzer şekilde, demirin paslanması, atmosferik nem ve oksijenin etkisiyle demir oksitlerin oluşumunu içerir. Korozyonun arkasındaki bilime bakarsak, metallerin oksitler, sülfürler, hidroksitler vb. gibi çok daha kararlı bir kimyasal bileşiğe dönüştüğü kendiliğinden / geri dönüşü olmayan bir süreç olduğunu söyleyebiliriz.
Korozyon Tanımı
Korozyon Nedir? Temel olarak, saf metallerin su veya hava gibi maddelerle reaksiyona girdiklerinde istenmeyen maddelere dönüşmesine neden olan doğal bir süreç olarak tanımlanır. Bu reaksiyon, metalin çevreye maruz kalan kısmından başlayarak metalin tüm kütlesine yayılmasına ve metalin hasar görmesine ve parçalanmasına neden olur.
Korozyon, metalin arzu edilen özelliklerini olumsuz yönde etkilediği için genellikle istenmeyen bir olgudur. Örneğin, demirin iyi gerilme mukavemetine ve sertliğine sahip olduğu bilinmektedir ( özellikle birkaç başka elementle alaşımlı ). Bununla birlikte, paslanmaya maruz kaldıklarında, demir nesneler kırılgan, pul pul ve yapısal olarak sağlam olmayan hale gelir. Öte yandan, korozyon difüzyon kontrollü bir süreçtir ve çoğunlukla açıkta kalan yüzeylerde meydana gelir. Bu nedenle, bazı durumlarda, maruz kalan yüzeyin aktivitesini azaltmak ve bir malzemenin korozyon direncini artırmak için girişimlerde bulunulur. Pasivasyon ve kromat dönüşümü gibi işlemler bu amaçla kullanılır. Bununla birlikte, bazı korozyon mekanizmaları her zaman görünür değildir ve daha az tahmin edilebilirdir.
Öte yandan, korozyon elektrokimyasal bir süreç olarak sınıflandırılabilir, çünkü genellikle metal ile su, oksijen, kükürt dioksit vb. gibi belirli atmosferik maddeler arasındaki redoks reaksiyonlarını içerir.
Tüm Metaller Korozyona Uğrar mı?
Demir, çinko vb. gibi reaktivite serisinde daha yükseğe yerleştirilen metaller çok kolay korozyona uğrar ve altın, platin ve paladyum gibi reaktivite serisinde daha düşük olan metaller korozyona uğramaz. Açıklama, korozyonun metallerin oksidasyonunu içermesi gerçeğinde yatmaktadır. Aşağı indikçe, reaktivite serilerinin oksitlenme eğilimi çok düşüktür ( oksidasyon potansiyelleri çok düşüktür ).
İlginç bir şekilde, alüminyum reaktif olmasına rağmen diğer metallerin aksine korozyona uğramaz. Bunun nedeni, alüminyumun zaten bir alüminyum oksit tabakası ile kaplı olmasıdır. Bu alüminyum oksit tabakası onu daha fazla korozyondan korur.
Korozyonu Etkileyen Faktörler
1. Metallerin CO2, SO2, SO3 gibi gazlar içeren havaya maruz kalması, ve saire.
2. Metallerin neme, özellikle tuzlu suya maruz kalması ( korozyon oranını arttırır ).
3. Tuz gibi safsızlıkların varlığı ( Örneğin, NaCl ).
4. Sıcaklık: Sıcaklıktaki bir artış korozyonu artırır.
5. Oluşan ilk oksit tabakasının doğası: Al2O3 gibi bazı oksitler daha fazla korozyonu önleyebilecek çözünmez bir koruyucu tabaka oluşturur. Pas gibi diğerleri kolayca parçalanır ve metalin geri kalanını açığa çıkarır.
6. Atmosferde asit varlığı: Asitler korozyon sürecini kolayca hızlandırabilir.
Korozyon Oranı
Deal - Grove modeli genellikle bir oksit tabakasının oluşumunu tanımlamak için kullanılır. Bu model, birçok farklı durumda oksit tabakası oluşumunu tahmin etmeye ve kontrol etmeye yardımcı olur. Bunun dışında korozyonu ölçmek için kilo verme yöntemi de kullanılmaktadır. Bu yöntemde, metalin veya alaşımın temiz, tartılmış bir parçası belirli bir süre korozif ortama maruz bırakılır. Bunu, korozyon ürünlerini ortadan kaldıran bir temizleme işlemi takip eder. Parça daha sonra ağırlık kaybını belirlemek için tartılır.
Korozyon oranı ( R ) şu şekilde hesaplanır:
R = kW/ρAt
Nerede
k = sabit,
W = t zamanında metalin ağırlık kaybı,
A = maruz kalan metalin yüzey alanı,
ρ metalin yoğunluğudur ( g/cm³ cinsinden ).
Korozyon Türleri
Korozyon türlerinden bazıları aşağıdakileri içerir:
( 1 ) Çatlak Korozyonu
Bir metalin herhangi iki yerel alanı arasında iyonik konsantrasyonda bir fark olduğunda, çatlak korozyonu olarak bilinen lokalize bir korozyon şekli meydana gelebilir. Örneğin, bu korozyon şekli çoğunlukla kapalı alanlarda ( yarıklar ) meydana gelir. Çatlak korozyonunun meydana gelebileceği alanlara örnek olarak contalar, rondelaların alt yüzeyi ve cıvata başları verilebilir. Tüm alüminyum alaşımları ve paslanmaz çelikler de çatlak korozyonuna maruz kalır. Bunun başlıca nedeni, yarıkların içinde korozyon oluşumuna yol açan diferansiyel bir havalandırma hücresinin oluşmasıdır.
( 2 ) Gerilme Korozyonu Çatlaması
Gerilme korozyonu çatlaması, 'SCC' olarak kısaltılabilir ve korozif ortam ve metal üzerine uygulanan çekme geriliminin bir sonucu olarak metalin çatlamasını ifade eder. Genellikle yüksek sıcaklıklarda oluşur.
Örneğin, klorür çözeltisi içinde östenitik paslanmaz çeliğin gerilme korozyonu çatlaması.
( 3 ) Taneler Arası Korozyon
Taneler arası korozyon, metal alaşımının katılaşması sırasında oluşan taneleri ayıran tane sınırlarındaki safsızlıkların varlığından dolayı oluşur. Bu tane sınırlarında alaşımın tükenmesi veya zenginleşmesi yoluyla da ortaya çıkabilir.
Örneğin, Alüminyum bazlı alaşımlar IGC'den etkilenir.
( 4 ) Galvanik Korozyon
Elektrokimyasal olarak farklı olan ve elektrolitik bir ortamda bulunan iki metal arasında bir elektrik teması olduğunda, galvanik korozyon ortaya çıkabilir. Bu metallerden birinin bir eklemde veya bir kavşakta bozunmasını ifade eder. Bu tür korozyona iyi bir örnek, tuzlu su ortamında bakır çelikle temas ettiğinde meydana gelen bozulma olabilir.
Örneğin, alüminyum ve karbon çeliği bağlandığında ve deniz suyuna daldırıldığında, alüminyum daha hızlı paslanır ve çelik korunur.
( 5 ) Çukur Korozyonu
Çukurlaşma Korozyonu çok tahmin edilemez ve bu nedenle tespit edilmesi zordur. En tehlikeli korozyon türlerinden biri olarak kabul edilir. Yerel bir noktada meydana gelir ve normal metalik yüzeyle çevrili bir korozyon hücresinin oluşumu ile ilerler. Bu 'çukur' oluştuktan sonra büyümeye devam eder ve çeşitli şekiller alabilir. Çukur, metale yüzeyden dikey yönde yavaşça nüfuz eder ve kontrol edilmezse sonunda yapısal arızaya yol açar.
Örneğin, çelik bir yüzey üzerinde bir su damlası düşünün, çukurlaşma su damlacığının merkezinde ( anodik bölge ) başlayacaktır.
( 6 ) Üniforma Korozyonu
Bu, metalin yüzeyine bir saldırının atmosfer tarafından gerçekleştirildiği en yaygın korozyon şekli olarak kabul edilir. Korozyonun boyutu kolayca fark edilebilir. Bu tür korozyon, malzemenin performansı üzerinde nispeten düşük bir etkiye sahiptir.
Örneğin, seyreltilmiş sülfürik aside batırılmış bir çinko ve çelik parçası genellikle tüm yüzeyinde sabit bir oranda çözülür.
( 7 ) Hidrojen Kanal Açma
Bu, aşındırıcı bir maddenin, aşınmış boru bileşenlerinin ve hidrojen gazı kabarcıklarının etkileşimi nedeniyle oluşan oluklar tarafından boruların korozyonudur. Kabarcıklar genellikle malzeme ile temas ettiğinde koruyucu kaplamayı çıkarır.
( 8 ) Metal Tozlama
Metal tozu, hassas malzemeler sentez gazı da dahil olmak üzere yüksek karbon aktivitelerine sahip belirli ortamlara maruz kaldığında ortaya çıkan zararlı bir korozyon şeklidir. Korozyon, dökme metalin metal tozuna parçalanmasına neden olur. Korozyon, buhar fazındaki karbon monoksitten ( CO ) metallerin yüzeyinde bir grafit tabakası biriktiğinde meydana gelir. Bu grafit tabakası daha sonra meta-kararlı M3C oluşturmaya devam eder. Genellikle metal yüzeyden uzaklaşan C türleri ( burada M bir metaldir ). Bazı durumlarda, M3C türleri gözlenebilir. Bu, metal atomlarının doğrudan grafit tabakasına aktarıldığı anlamına gelir.
( 9 ) Mikrobiyal Korozyon
Mikrobiyolojik olarak etkilenmiş korozyon ( MIC ) olarak da bilinen mikrobiyal korozyon, mikroorganizmaların neden olduğu bir korozyon türüdür. En yaygın olanı kemoototroflardır. Oksijen varlığında veya yokluğunda hem metalik hem de metalik olmayan malzemeler bu korozyondan etkilenebilir.
( 10 ) Yüksek Sıcaklık Korozyonu
Yüksek sıcaklık korozyonu, adından da anlaşılacağı gibi, ısınma nedeniyle malzemelerin ( çoğunlukla metallerin ) bir tür korozyonudur. Oksijen, kükürt veya diğer bileşikler gibi gazlar içeren sıcak bir atmosfer nedeniyle metalin kimyasal bozulması meydana gelebilir. Bu bileşikler, malzemeleri ( bu durumda metalleri ) kolayca oksitleyebilir. Örneğin, araba motorlarında kullanılan malzemeler, aşındırıcı yanma ürünleri içeren bir atmosferden etkilenebilecekleri yüksek sıcaklıklarda uzun sürelere dayanmak zorundadır.
Korozyon Örnekleri, Reaksiyonları ve Etkileri
İşte çoğunlukla metallerde görülen bazı tipik korozyon örnekleri.
1. Bakır Korozyonu
Bakır metali çevreye maruz kaldığında atmosferdeki oksijenle reaksiyona girerek kırmızı renkli bakır ( I ) oksit oluşturur.
2Cu(s) + ½ O2(g) → Cu2O(s)
Cu2O ayrıca siyah renkli CuO'yu oluşturmak üzere oksitlenir.
Cu2O(s) + ½ O2(g) → 2CuO(s)
Bu CuO, CO2, SO3 ile reaksiyona girer ve H2O atmosferde bulunur ve oluşturur. Cu2(OH)2(s) ( Malakit ), mavi renkli ve Cu4SO4(OH)6(s) ( Brochantite ), yeşil renktedir.
Bu nedenle bakırın mavimsi - yeşil renge dönüştüğünü gözlemliyoruz.
Bunun tipik bir örneği, üzerinde mavi-yeşil renge dönüşen bakır kaplamaya sahip olan Özgürlük Anıtı'nın rengidir.
2. Gümüş Karartma
Gümüş, havadaki kükürt ve kükürt bileşikleri ile reaksiyona girerek gümüş sülfür (Ag2S), siyah renktedir. Açıkta kalan gümüş formları Ag2H ile reaksiyona girerken H2S(g) şeklinde değiştirilmiştir. Belirli endüstriyel işlemler nedeniyle mevcut olan atmosferde.
2Ag(s) + H2S(g) → Ag2S(s) + H+2+(g) şeklinde değiştirilmiştir.
3. Demirin Korozyonu ( Paslanma )
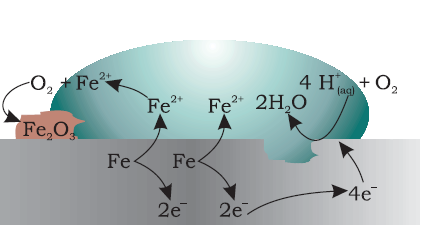
En sık görülen örnek olan demirin paslanması, demirin hava veya su ile temas etmesiyle meydana gelir. Reaksiyon, tipik bir elektrokimyasal hücre reaksiyonu olarak görülebilir. Aşağıda verilen şemayı göz önünde bulundurun.
Burada metal demir elektron kaybeder ve Fe{aq}2+ 'ya dönüşür ( bu anot pozisyonu olarak düşünülebilir ). Kaybedilen elektronlar, Hiyonlarla birleştikleri diğer tarafa hareket edecektir. Hion'lar H++2O tarafından serbest bırakılır veya H2CO3 tarafından ( Yardımcı Firma ) atmosferde bulunur ( bu katot konumu olarak düşünülebilir ).
H2O ⇋ H+ + OH−
H2CO3 ⇋ 2H+ + CO23
Böylece H ve elektronların reaksiyonu ile oluşan Hidrojen, oksijenle reaksiyona girerek H+2O oluşturur.
Anot reaksiyonu
2Fe(s) → 2Fe2+ + 4e−;
E0Fe2+/Fe = -0.44V
Katot reaksiyonu
O2(g) + 4H+(aq) + 4e− 2→ H2O(l)E0H+/O2/H2/O = 1.23V
Genel reaksiyon
2Fe(s) + O2(g) + 4H+(aq) → 2Fe2+(aq) + H2O(l)E0cell = 1.67V
Fe2+ Anotta oluşan iyonlar atmosferdeki oksijenle reaksiyona girerek Fe3+ 'ya oksitlenir ve Fe2O3 'ün oluşturulması, hidratlı formda Fe2O3xH2O olarak ortaya çıkar.
Fe2+ + 3O2 → 2Fe2O3
Fe2O3 + xH2O → Fe2O3. xH2O ( pas )
Diğer örnekler şunları içerir:
- Çinkonun oksijen ve HCl ile reaksiyona girerek beyaz renkli ZnCl2 oluşturduğunda korozyonu.
- Kalayın siyah renkli Na2[Sn(OH)2] oluşturmak için korozyonu.
Efektleri
Korozyonun birçok şey üzerinde değişen derecelerde etkisi olabilir. Bu nedenle, esas olarak doğal kaynakların israfına neden olur. Ek olarak, bina yapılarının zayıflaması ve dengesiz hale gelmesi, aşınmış parçaların neden olduğu kazaların yanı sıra çatlamış boru hatları, köprü çökmesi, nakliye aracı kazaları veya diğer felaketler gibi diğer istenmeyen arızalar gibi tehlikeli durumlara da neden olabilir. Bu nedenle, her ne pahasına olursa olsun korozyonu kontrol etmek ve önlemek önemlidir.
Korozyonun Önlenmesi
Büyük kayıpları önlemek için korozyonun önlenmesi son derece önemlidir. Gördüğümüz ve kullandığımız yapıların çoğu metallerden yapılmıştır. Buna köprüler, otomobiller, makineler, pencere ızgaraları, kapılar, demiryolu hatları vb. gibi ev eşyaları dahildir. Bu endişe verici bir konu olsa da, metalik nesnelerde korozyon hasarını yavaşlatmak veya önlemek için çeşitli işlemler kullanılır. Bu, özellikle havaya, tuzlu suya, asitlere veya diğer düşmanca ortamlara sıklıkla maruz kalan malzemelere yapılır. Korozyonu önlemek için popüler yöntemlerden bazıları şunlardır:
- Galvanik
- Eloksal
- Pasivasyon
- Biyofilm Kaplamalar
- Korozyon Önleyici Koruyucu Kaplamalar
- Boyama ve yağlama
- Korozyon İnhibitörü veya Kurutma Maddelerinin Kullanımı
- Metal Yüzeyin Periyodik Temizliği
Korozyon Hakkında Sıkça Sorulan Sorular
1. Korozyon nedir?
Korozyon, metalin daha kararlı bir kimyasal okside dönüştürülmesinin doğal bir olgusudur.
2. Tüm metaller paslanır mı?
Hayır, tüm metaller korozyona uğramaz. Reaktivite serisinde daha yüksek olan metaller oksidasyon potansiyelleri yüksek olduğu için kolayca korozyona uğrarlar. Örneğin, demir.
3. Korozyonu ne etkiler?
Havaya veya neme ( tuzlu su ) maruz kalan metaller korozyonu arttırır.
4. Sıcaklığın korozyona etkisi nedir?
Korozyon, sıcaklık arttıkça artar.
5. Yüksek sıcaklık korozyonu ile ne kastedilmektedir?
Isınma nedeniyle metallerin korozyonuna yüksek sıcaklık korozyonu denir.